Kontakt:Errol Zhou (Hr.)
Tlf.: plus 86-551-65523315
Mobil/WhatsApp: plus 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
E-mail:sales@homesunshinepharma.com
Tilføje:1002, Huanmao Bygning, Nr.105, Mengcheng Vej, Hefei By, 230061, Kina
Novartis offentliggjorde for nylig de detaljerede resultater af den centrale fase III REACH3-undersøgelse (NCT03112603) på det 62. Dette er en randomiseret, open-label, multi-center undersøgelse udført hos børn (≥12 år) og voksne patienter, der udvikler steroid-ildfaste eller steroid-afhængige kronisk graft-versus-host sygdom (GvHD) efter allogen stamcelletransplantation . Dataene viser, at sammenlignet med den bedste tilgængelige behandling (BAT), oral JAK1/2-hæmmer Jakavi (ruxolitinib) væsentligt forbedret en række effektindikatorer hos patienter med steroid ildfast/ afhængig kronisk GvHD, herunder svigt-fri overlevelse (FFS) ) Og symptomerne rapporteret af patienten.
Kronisk GvHD er en livstruende komplikation af stamcelletransplantation, og omkring halvdelen af patienterne vil udvikle steroid ildfast/afhængighed. Det er værd at nævne, at Jakavi er det første lægemiddel til at vise effektivitet i behandlingen af steroid-ildfaste/afhængige kroniske GvHD i store randomiserede kliniske forsøg. Ifølge resultaterne af REACH3-undersøgelsen planlægger Novartis at indsende en lovgivningsmæssig ansøgning til Jakavi om behandling af steroid-ildfaste/afhængige GvHD-patienter i lande uden for USA i Europa i første halvdel af 2021.
Dr. Robert Zeiser, Institut for Hæmatologi, Onkologi og Stamcelletransplantation, University Hospital i Freiburg, Tyskland, sagde: "Den destruktive og potentielt fatale virkning af kronisk GvHD efter stamcelletransplantation har bragt enorme udfordringer til behandling, især for næsten halvdelen af patienterne. For patienter, der ikke har tilstrækkeligt reageret på steroid terapi. Baseret på de overbevisende REACH3-undersøgelsesresultater har vi nu en potentiel ny standard for pleje af disse patienter."
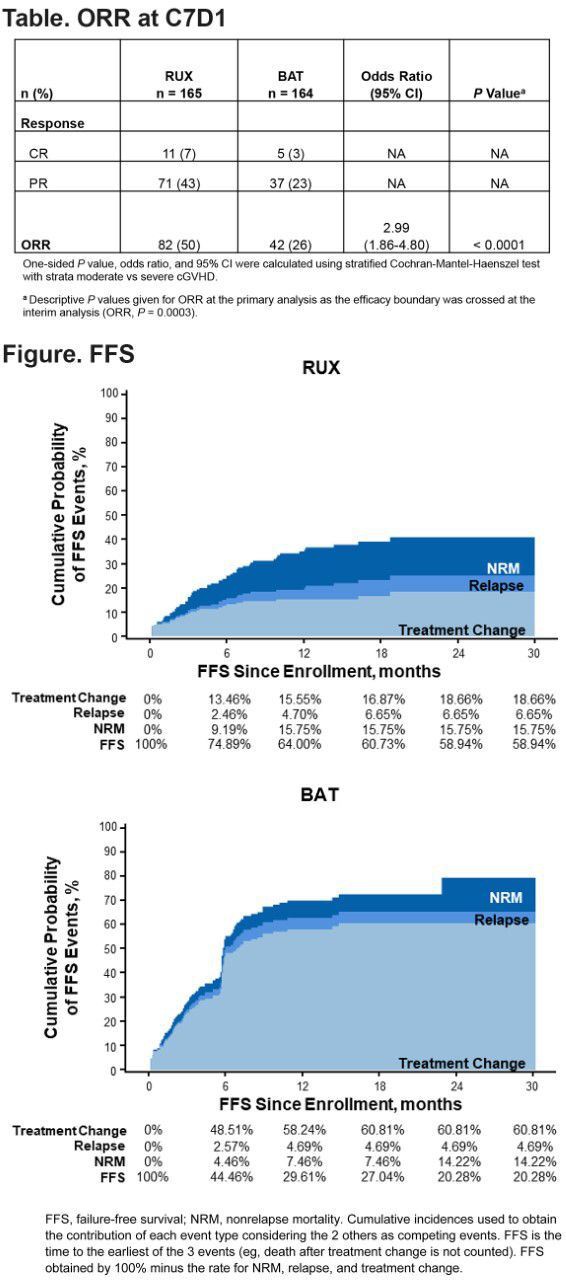
I REACH3-undersøgelsen, ved den 24.<0.0001). in="" addition,="" jakavi="" also="" showed="" statistically="" significant="" and="" clinically="" significant="" improvements="" in="" key="" secondary="" endpoints:="" (1)="" compared="" with="" the="" bat="" group,="" the="" jakavi="" group="" had="" failure-free="" survival="" (ffs;="" defined="" as="" early="" relapse="" of="" the="" disease="" and="" initiation="" of="" new="" systemic="" therapy="" treatment="" of="" chronic="" gvhd,="" death="" of="" death)="" showed="" significant="" improvement="" (median="" ffs:="" less="" than="" 5.7="" months;="" hr="0.370;" 95%ci:="" 0.268-0.510;=""><0.0001). (2)="" according="" to="" the="" modified="" lee="" symptom="" score="" (mlss)="" scale,="" the="" ratio="" of="" responders="" whose="" total="" symptom="" score="" (tss)="" was="" reduced="" by="" ≥7="" points="" from="" baseline="" was="" used="" to="" evaluate.="" the="" symptoms="" reported="" by="" patients="" in="" the="" jakavi="" group="" were="" more="" improved="" than="" those="" in="" the="" bat="" group="" (24.2%="" vs="" 11.0%;="" p="0.0011)." (3)="" 76.4%="" of="" patients="" in="" the="" jakavi="" group="" achieved="" the="" best="" overall="" response="" (bor),="" and="" 60.4%="" in="" the="" bat="" group="" (or="2.17;" 95%ci:="" 1.34-3.52).="" the="" median="" duration="" of="" response="" (dor)="" has="" not="" been="" reached="" in="" the="" jakavi="" group,="" and="" 6.24="" months="" in="" the="" bat="">
I denne undersøgelse blev der ikke observeret nye sikkerhedssignaler, og bivirkninger forårsaget af behandlingen var i overensstemmelse med Jakavi' kendte sikkerhed. De mest almindelige bivirkninger i Jakavi-gruppen og BAT-gruppen var anæmi (29,1 % vs. 12,7 %), trombocytopeni (21,2 % vs. 14,6 %), forhøjet blodtryk (15,8 % vs. 12,7 %) feber (15,8 % mod 9,5 %). Selv om 37,6 % og 16,5 % af patienterne krævede dosisjusteringer af Jakavi og BAT, var antallet af patienter, der ophørte med behandlingen på grund af AEs, lavt (henholdsvis 16,4 % og 7 %). Dødeligheden var den samme på tværs af behandlingsgrupper (19% vs 16% BAT). Antallet af dødsfald forårsaget af kronisk GvHD i Jakavi-gruppen var lidt højere.
Graft versus host sygdom (GvHD) er en fælles og potentielt livstruende komplikation efter allogen stamcelletransplantation. Det er en reaktion fra donorceller, der angriber modtagerens normale celler, fordi donorcellerne betragter recipientcellerne som fremmede celler. De to hovedtyper af GvHD er akut GvHD (forekommer inden for 100 dage efter transplantation) og kronisk GvHD (forekommer inden for 100 dage efter transplantation). Efter allogen stamcelletransplantation, ca 50% af patienterne vil opleve akut eller kronisk GvHD, eller begge dele. Symptomerne på kronisk GvHD kan påvirke huden, mave-tarmkanalen, lever, mund, lunger, og led. For patienter, der ikke reagerer på indledende steroid behandling eller betragtes ildfaste til steroid terapi, yderligere behandlingsmuligheder er presserende behov for.
Resultaterne af REACH3-undersøgelsen supplerer de tidligere rapporterede positive resultater af den centrale fase III REACH2-undersøgelse af Jakavi til behandling af akut GvHD. Sidstnævnte er den første fase III-undersøgelse, der med succes opnår det primære endepunkt i behandlingen af akut GvHD. Dataene viser: og den bedste tilgængelige behandling Sammenlignet med (BAT), Jakafi væsentligt forbedret en række effektindikatorer hos patienter med steroid ildfast akut GvHD.
I maj 2019 godkendte den amerikanske FDA ruxolitinib (markedsført af Incyte i USA under handelsnavnet Jakafi) baseret på resultaterne af enarmsfasen II REACH1-undersøgelse til brug hos børn og voksne patienter på 12 år og derover til behandling af steroid-ildfast akut Graft versus host disease (GvHD). Det er værd at nævne, at ruxolitinib er det første lægemiddel godkendt af FDA til behandling af steroid-ildfaste GvHD. I REACH1-undersøgelsen var den samlede responsrate (ORR) for ruxolitinib på den 28.
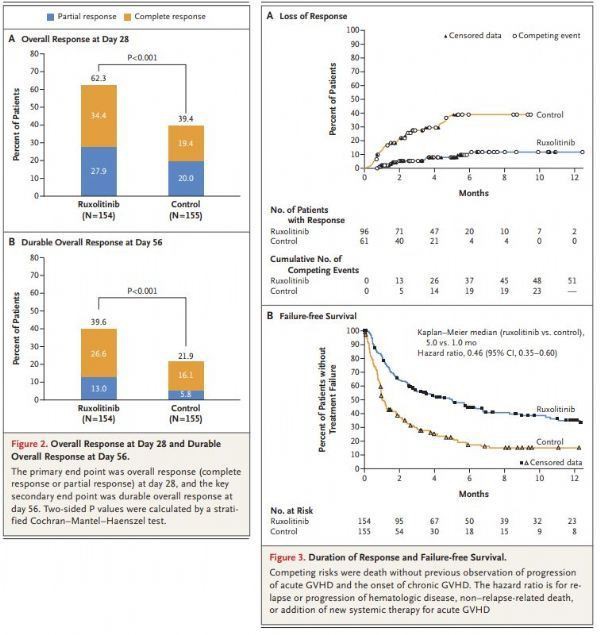
I april i år blev resultaterne af REACH2-undersøgelsen offentliggjort i New England Journal of Medicine (NEJM): Sammenlignet med BAT-behandlingsgruppen blev den samlede responsrate (ORR) for Jakavi-behandlingsgruppen på dag 28 væsentligt forbedret (62 % mod 39 %, p<0.001), the="" primary="" endpoint="" of="" the="" study="" was="" reached.="" in="" terms="" of="" key="" secondary="" endpoints,="" compared="" with="" the="" bat="" treatment="" group,="" the="" proportion="" of="" patients="" in="" the="" jakavi="" treatment="" group="" who="" maintained="" a="" durable="" orr="" within="" 8="" weeks="" was="" significantly="" higher="" (40%="" vs="" 22%,=""><0.001). in="" addition,="" the="" failure-free="" survival="" (ffs)="" of="" the="" jakavi="" treatment="" group="" was="" longer="" than="" that="" of="" the="" bat="" treatment="" group="" (5.0="" months="" vs="" 1.0="" months;="" hr="0.46," 95%ci:="" 0.35,="" 0.60),="" and="" other="" secondary="" endpoints="" also="" showed="" positive="" trends,="" including="" remission="" duration="">
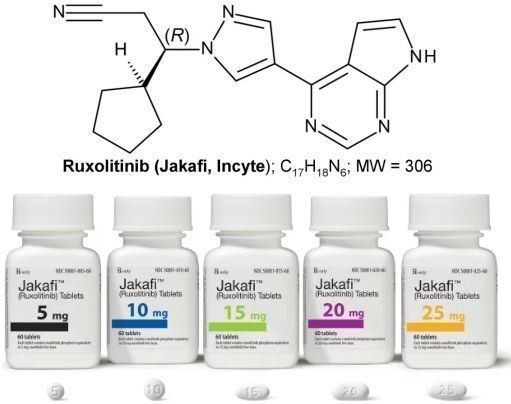
ruxolitinib er den første mundtlige Janus kinase 1 og Janus kinase 2 (JAK1/JAK2) hæmmer. Lægemidlets nuværende indikationer omfatter: knoglefibrose, polycythemia vera (PV), kortikosteroid-ildfast akut transplantat versus værtssygdom (GvHD). På det amerikanske marked, stoffet er stemplet som Jakafi og sælges af Incyte; uden for USA, stoffet er mærkevarer som Jakavi og sælges af Novartis.
I øjeblikket er Incyte også ved at udvikle ruxolitinib creme, som er i fase III klinisk udvikling: (1) til behandling af patienter med mild til moderat atopisk dermatitis (TRuE-AD projekt), (2) til behandling af unge og voksne Vitiligo (TRuE-V Project). Incyte har de globale rettigheder til at udvikle og kommercialisere ruxolitinib creme. De tidligere offentliggjorte fase II-studiedata viste, at sammenlignet med gruppen af køretøjskontrol (lægemiddelfri creme) havde patienter i ruxolitinib cremebehandlingsgruppen signifikant forbedret scorer i ansigtets vitiligo-sværhedsgrad, og systemiske vitiligo hudlæsioner (repigmentering) Har en betydelig forbedring. I februar i år var fase III-projektet af ruxolitinib creme til behandling af atopisk dermatitis vellykket.